Tak jako Homocystinurie je vzácné genetické metabolické onemocnění, které je způsobeno nedostatkem enzymů a vyznačuje se zvýšenou koncentrací homocysteinu v krvi. Při včasné a důsledné terapii lze homocystinurii obvykle léčit dobře.
Co je homocystinurie?

© Anastasia Okhrimenko - stock.adobe.com
Tak jako Homocystinurie je vzácné, geneticky způsobené onemocnění metabolismu aminokyselin, které je způsobeno poruchami různých enzymů podílejících se na metabolismu methioninu (esenciální aminokyselina).
Homocystein a homocystin jsou produkty rozkladu nebo meziprodukty tohoto metabolického procesu a jsou u zdravých lidí okamžitě metabolizovány. Vzhledem k přítomnosti vadných enzymů je to možné pouze u těch, které jsou ovlivněny homocystinurií, jen v omezené míře, takže se zvyšuje koncentrace homocysteinu v krvi a homocystinu v moči.
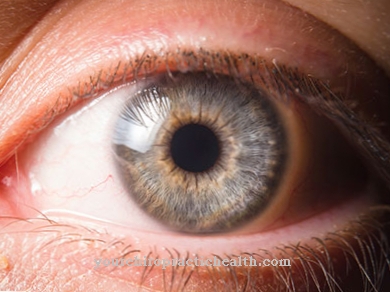
Zvýšená koncentrace těchto toxických aminokyselin může vést k poškození různých orgánových systémů. Oční choroby (dislokace čoček, myopie, glaukom), změny skeletu (osteoporóza, marfanoidní dlouhé končetiny), poškození centrálního nervového systému (mentální a fyzická retardace, křeče, cerebrovaskulární poruchy) a cévní systém (tromboembolismus, cévní okluze) jsou charakteristické následky homocystinurie.
příčiny
Homocystinurie je způsobena autozomálně recesivní dědičnou genetickou vadou, která vede k nedostatku různých enzymů zapojených do metabolismu methioninu. V závislosti na specificky ovlivněném enzymu a částečném procesu metabolismu methioninu se rozlišují tři formy homocystinurie.
Čím častěji Typ I. V homocystinurii je nedostatek enzymu cystathion beta syntáza (CBS), který narušuje syntézu cysteinu z methioninu. Výsledkem je, že se homocystein hromadí v krvi (hyperhomocysteinémie) a homocystin se hromadí v moči (homocystinurie).
Typ II Homocystinurie se vyznačuje nedostatkem 5,10-methylenetetrahydrofolát reduktázy (MTHFR), která reguluje syntézu methioninu z homocysteinu. Tento metabolický dílčí proces je tedy u pacientů s typem II narušen a kromě obohacení séra homocysteinem může také vést k nedostatku methioninu.
Typ III homocystinurie se vyznačuje nedostatkem kobalaminu (koenzym vitamín B12). Cobalamin se také podílí na syntéze methioninu z homocysteinu, takže nedostatek může také vést ke zvýšené koncentraci homocysteinu v krvi a k nedostatku metioninu.
Příznaky, onemocnění a příznaky
Homocystinurie se může vyskytovat v různých formách. Příznaky jsou rozmanité a liší se v závislosti na stádiu života. Před dosažením věku dvou let se příznaky onemocnění objevují pouze ve výjimečných případech. Kromě charakteristických laboratorních nálezů jsou novorozenci s homocystinurií normální.
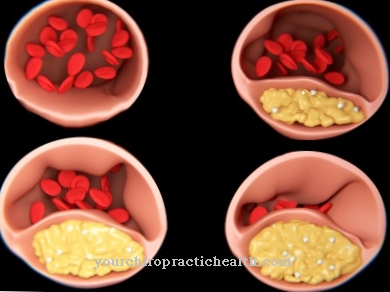
Hladina homocysteinu v krvi je obvykle významně zvýšena. To poškozuje krevní cévy, což může v dlouhodobém horizontu vést ke kalcifikaci cév (arterioskleróza) a tím k embolii a trombóze. V důsledku toho je délka života postižených výrazně omezena. Nejviditelnějším příznakem metabolické poruchy u dětí je prolaps oční čočky.
To je často spojeno s krátkozrakostí. Čím dříve se objeví první příznaky nemoci, tím vyšší je riziko psychomotorické retardace (mentální postižení), což je nevratné. Většina postižených již trpí osteoporózou v dětství. Páteř se zplošťuje a postupně se deformuje.
Vysoká hladina homocysteinu často vede k vysoké postavě a symptomům, které mohou být podobné Marfanovu syndromu. Patří mezi ně například přítomnost kuřecího a trychtýřového prsu, posunuté oční čočky (luxace čočky nebo ektopie čočky), glaukom (glaukom), odchlípení sítnice a pavoučí prsty (arachnodaktyly).
Diagnóza a průběh
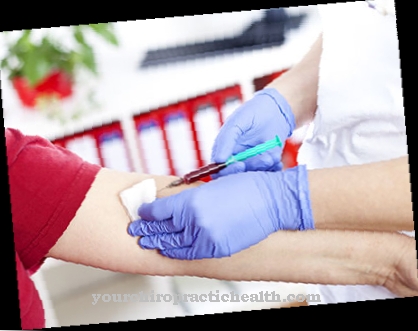
Diagnostikovat Homocystinurie používají se různé laboratorní analýzy. Pokud analýza moči (např. Test kyanid-nitroprusid) odhalí zvýšenou koncentraci homocystinu a / nebo sníženou koncentraci methioninu (typy II a III), může to znamenat homocystinurii.
Krevní analýzu lze použít ke stanovení koncentrace homocysteinu v séru a diagnostice hyperhomocysteinémie spojené s homocystinurií. Diagnóza je potvrzena kultivací buněk ze vzorku pojivové tkáně nebo tkáně jater, přičemž základní genetický defekt může být detekován přímo.
Průběh homocystinurie se může u jednotlivých osob lišit, pokud jde o příznaky a sekundární onemocnění. Při včasné diagnóze a časném zahájení léčby má homocystinurie obvykle příznivý průběh a dobrou prognózu.
Komplikace
Homocystinurie vede především k závažným psychologickým potížím, které mohou mít extrémně negativní dopad na život pacienta a každodenní život. Ve většině případů se vyskytuje silná porucha osobnosti, která je doprovázena poruchami chování. Tyto poruchy mohou vést k závažným komplikacím, zejména u dětí.
Pacient je zpravidla postižen sociálním vyloučením a ze života se stále více stahuje. Není neobvyklé, že to vede k depresivním náladám. Kromě toho jsou v očích nepohodlí, takže se může vyvinout například glaukom nebo krátkozrakost. Mnohá onemocnění krevních cév se objevují také mnohem dříve, a proto mohou vést k omezením pohybu.
Léčba sama o sobě zpravidla nevede ke zvláštním komplikacím a provádí se pomocí drog. Toto onemocnění postupuje pozitivně relativně rychle. Ve většině případů neexistují žádné další příznaky ani po léčbě. Včasná léčba nesnižuje délku života. Psychologické stížnosti může psycholog řešit podpůrně.
Kdy byste měli jít k lékaři?
Pokud se objeví příznaky, jako jsou poruchy chování, trombóza nebo zpoždění ve vývoji, měl by být rozhodně lékař. Příznaky osteoporózy nebo arteriosklerózy by měly být také objasněny v rané fázi. Lékař musí určit příčinu příznaků a v případě potřeby zahájit léčbu. Proto by se uvedené příznaky měly rychle vyjasnit. Lidé s genetickou vadou jsou zvláště náchylní k rozvoji homocystinurie. Dotčené osoby by měly pečlivě konzultovat svého rodinného lékaře a informovat je o všech neobvyklých příznacích.
V zásadě je třeba objasnit stížnosti, které přetrvávají déle než několik dní nebo které zvyšují intenzitu po delší časové období. Charakteristické příznaky homocystinurie se obvykle vyvíjejí zákeřně a často se objevují pouze tehdy, pokud již nastaly nevratné choroby. O to důležitější je rozpoznat včasné příznaky a nechat je léčit. Lidé, kteří si sami nebo jiné osoby všimnou fyzických nebo mentálních změn, které mohou souviset s metabolickými poruchami, by se měli co nejdříve obrátit na svého rodinného lékaře. Dalšími kontaktními osobami jsou specialisté na interní medicínu nebo specializovaná klinika pro dědičná onemocnění.
Lékaři a terapeuti ve vaší oblasti
Léčba a terapie
Terapie Homocystinurie závisí na základním typu onemocnění nebo defektu enzymu a jeho cílem je snížit a eliminovat zvýšenou koncentraci toxického homocysteinu. Homocystinurie typu I je ošetřena pyridoxinem (vitamin B6), pokud existuje zbytková aktivita defektního enzymu.
Látka zvyšuje enzymatickou aktivitu a snižuje koncentraci homocysteinu v krvi. Asi 50 procent osob postižených tímto typem velmi dobře reaguje na orální terapii vysokými dávkami vitaminu B6. Kromě toho se na podporu terapie doporučuje dieta s nízkým obsahem methioninu a s vysokým obsahem cystinu.
Pokud v homocystinurii typu II a III existuje zbytková enzymatická aktivita, při které je narušena syntéza methioninu z homocysteinu, jsou provedeny pokusy o omezení poškození kobalaminovými přípravky (vitamin B12). Pro obě formy homocystinurie je indikována strava bohatá na methionin.
Kyselina listová, která má také pozitivní účinek na aktivitu defektní 5,10-methylenetetrahydrofolát reduktázy, jakož i methioninu a betainu, se terapeuticky používá pro typ II. Antikoagulancia (kyselina acetylsalicylová) se používají k prevenci cévních onemocnění, jako je trombóza a embolie.
Výhled a předpověď
Při včasné diagnostice a intenzivní terapii je prognóza homocystinurie obvykle příznivá. Nemoc není léčitelná, protože se jedná o genetický defekt. V rámci terapie je však možné trvale snížit koncentraci homocysteinu a methioninu, což významně snižuje pravděpodobnost vývojových poruch a komplikací.
Stupeň závažnosti homocystinurie se může lišit. Existují formy nemoci, které jsou zpočátku normální a jinak mírné. I zde však od 20 nebo 30 let existuje větší riziko rozvoje arteriosklerózy, trombózy, embolie, srdečních záchvatů a mozkových příhod.
Pokud je však koncentrace homocysteinu již v kojeneckém věku velmi vysoká, existuje u dítěte bez intenzivní léčby velké riziko poruch fyzického a duševního vývoje. Duševní postižení se může projevit již v prvních dvou letech života. Postižené děti často trpí také osteoporózou. Až 70 procent neléčených dětí se vyvine v očních problémech, které jsou nejjasněji vyjádřeny v prolapsu oční čočky. Mezi další důsledky pro oči patří glaukom, extrémní krátkozrakost, odchlípení sítnice a slepota. Pokud jsou těžké formy onemocnění léčeny příliš pozdě nebo vůbec, budou se trombózy a embolie rozvíjet u 30 procent všech pacientů mladších 20 let.
prevence
Tam Homocystinurie je genetické onemocnění, kterému nelze zabránit. Pokud je však léčba zahájena brzy, lze komplikacím homocystinurie zabránit nebo je omezit. Kromě toho mají postižené osoby možnost nechat své nenarozené dítě testovat na homocystinurii v rámci prenatální diagnostiky (analýza plodové vody). Sourozencům postižených se také doporučuje zkontrolovat homocystinurii.
Následná péče
V závislosti na typu enzymatické vady, která je příčinou metabolické poruchy, je celá řada opatření užitečná a nezbytná jako součást následné péče o homocystinurii. U homohystinurie typu I musí pacient kromě lékařského podávání vitaminu B6 dodržovat dietu bohatou na vitamíny. Vitamin B6 zvyšuje aktivitu defektního enzymu a následně vede k nižší koncentraci homocysteinu v krvi.
Aby byl tento účinek zachován, musí být strava trvale dodržována. Totéž platí pro spotřebu potravin bohatých na cystiny a nízkého obsahu methioninu. U homocystinurie typu II musí dieta pokračovat, aby se dosáhlo dlouhodobých účinků. Během následné kontroly se navíc provádějí pravidelné kontroly. Lékař musí zkontrolovat aktivitu postižených enzymů av případě potřeby upravit terapii.
Protože homocystinurie obvykle není vážným onemocněním, postačují lékařské kontroly každé tři až šest měsíců. V případě závažných poruch by měl být odborník konzultován měsíčně po dokončení skutečné terapie. Kromě toho je třeba věnovat pozornost neobvyklým příznakům, protože metabolická porucha může z dlouhodobého hlediska způsobit další onemocnění, která musí být léčena.
Můžete to udělat sami
V závislosti na typu defektu enzymu, který je základem homocystinurie a na jaké terapii lékař používá, může pacient udělat několik věcí, aby zmírnil příznaky.
Především je důležitá strava bohatá na cystiny. Oběť by měla konzumovat hlavně rýži, ořechy, sójové boby a ovesné produkty. Účinná látka se nachází také ve vodních melounech, slunečnicových semenech a zeleném čaji. Lékař také předepíše doplňky vitamínu B12, aby se omezilo poškození. Dotčená osoba může tato opatření podpořit vytvořením výživového plánu bohatého na metiony spolu s odborníkem na výživu a jeho důsledným prováděním. Je třeba se vyvarovat potravin s vysokým obsahem bílkovin, jako jsou vejce nebo maso. Potraviny s nízkým obsahem bílkovin jsou povoleny, včetně ovoce, zeleniny a těstovin s nízkým obsahem bílkovin, chleba nebo mouky ze specializovaných obchodů. Tato strava by měla být podporována různými vitaminy B a kyselinou listovou.
Po vymizení nemoci by měl pacient podstoupit další prohlídky. Homocystinurie je celoživotní onemocnění, které vyžaduje pravidelné hodnocení ve specializovaném léčebném centru. Důkladné sledování umožňuje identifikovat a léčit metabolické problémy v rané fázi před vznikem komplikací.

.jpg)
.jpg)

.jpg)


.jpg)



.jpg)





.jpg)
.jpg)

.jpg)