Biokatalyzátor Sulfit oxidáza způsobuje přeměnu toxických sloučenin síry z rozkladu aminokyselin na netoxické sulfáty.
Je to životně důležité, a proto se vyskytuje ve všech organismech. Pokud je jeho funkce narušena genetickou vadou, dochází k nedostatku sulfitové oxidázy. Příliš vysoký obsah siřičitanu v krvi může mít také negativní účinky u jinak zdravých pacientů.
Co je to sulfit oxidáza?
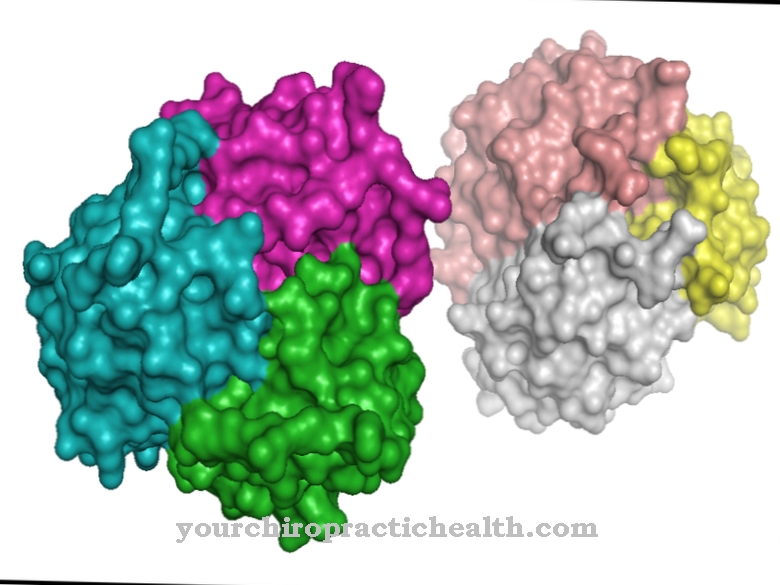
Sulfit oxidáza (název genu: SUOX) je název enzymu obsahujícího molybden, který se skládá ze 466 aminokyselin. Patří do rodiny xantin dehydrogenáz a nachází se téměř ve všech organismech. Ve svém středu obsahuje molybden, důležitý stopový prvek.
Kov se zde vyskytuje ve své biologicky dostupné formě jako molybdenanový anion. Sulfit oxidáza ji používá jako kofaktor (molybdenan-molybdopterinová sloučenina). Enzym přeměňuje aminokyseliny methionin, cystein, atd., Které obsahují síru a které jsou přijímány potravou, na neškodné sirné soli (sírany), které se poté vylučují močí. U savců se biokatalyzátor degradující síru vyskytuje primárně v játrech a ledvinách. Enzym sulfit oxidáza zajišťuje, že krevní kyslík se kombinuje s esenciálními aminokyselinami a dalšími látkami síry.
Uvolněné elektrony se používají prostřednictvím transportního řetězce elektronů k produkci ATP (adenosintrifosfát). Enzym katalyzuje 10 krát množství siričitanů na litr alkoholu.
Funkce, efekt a úkoly
Každý den konzumuje proteiny a potravinářské přídatné látky obsahující síru. Ty jsou obsaženy například v nakládané zelenině, grapefruitové šťávě atd. A jsou určeny k ochraně potravin před mikrobiálním napadením a změnou barvy. Ve víně vytvářejí kytičné látky.
Rozklad samotného cysteinu má za následek 1680 mg toxického siřičitanu v těle každý den, který musí být okamžitě přeměněn sulfitovou oxidázou, aby nedošlo k poškození orgánů a tkání. Enzym pracuje společně s jinými biokatalyzátory. Sulfity jsou jedovaté a mohou ničit životně důležité látky v těle a inhibovat potřebné metabolické procesy i v nejmenším množství. Aby bylo možné provést důležitou detoxikaci buněk, potřebuje siřičitanová oxidáza stopový prvek molybden.
Nedostatek tohoto kovu může vést k vážným následkům. Příliš vysoký obsah rtuti v těle může také inhibovat funkčnost sulfit oxidázy.
Vzdělávání, výskyt, vlastnosti a optimální hodnoty
Sulfit oxidáza je produkována hlavně v mitochondriích, „energetických centrech“ buněk. U potkanů se například 80% vyskytuje v mitochondriích jaterních buněk. Kromě toho je stále silně zastoupena v buňkách ledvin.
Oxid molybdeničitý potřebný pro aktivitu sulfit oxidázy se nachází v aktivním centru enzymu. Jak vědci nedávno objevili, nanočástice oxidu molybdenového mohou jej nahradit u pacientů s nedostatkem molybdenu. Mají podobný katalytický účinek v těle jako přírodní enzym. Tímto způsobem by mohla být léčena dříve fatální onemocnění, jako je sulfocysteinurie.
Nemoci a poruchy
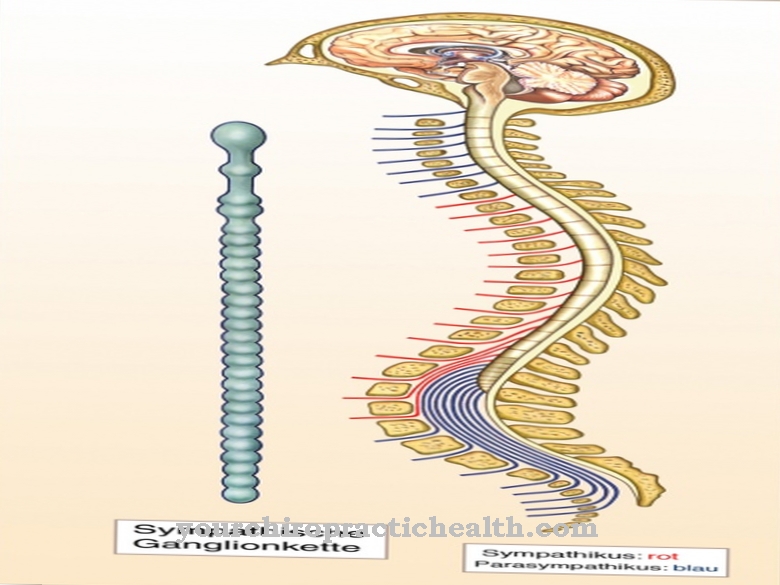
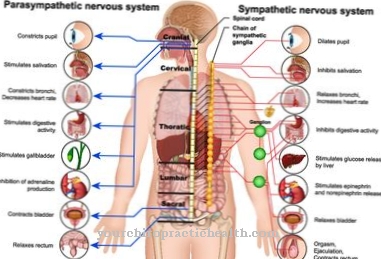
Nedostatek sulfit oxidázy může u jinak zdravých lidí způsobit astmatické a dokonce anafylaktické reakce, protože parasympatický nervový systém ovlivňuje žírné buňky odpovědné za vývoj alergií.
Kromě toho, pokud je hladina sulfit oxidázy příliš nízká, může to vést k těžké únavě, bolestem hlavy a nízkým hladinám cukru v krvi. Genetický nedostatek v životně důležitém enzymu má však ještě horší důsledky. Novorozenec se rodí s fyzickými deformacemi a mentálním postižením. Tento tzv. Nedostatek sulfitové oxidázy nebo sulfocysteinurie se vyskytuje jako onemocnění s deficitem kofaktoru molybdenu (MoCo) při odhadovaném počtu 100 000 až 500 000 narození. Kojenci trpící izolovaným defektem sulfitové oxidázy vykazují podobné příznaky: těžkou encefalopatii, sotva kontrolovatelné záchvaty, spasticitu, mikrocefalii, uvolnění svalů a progresivní mozkovou atrofii.
Protože autozomálně recesivní zděděné onemocnění s nedostatkem enzymů nelze v současné době účinně léčit, drobní pacienti obvykle umírají v dětství: sirné sloučeniny, které se nerozkládají na neurony jedu a myelinové pláště centrálního nervového systému a jsou ukládány v buněčné tkáni. I po narození jsou problémy s jídlem a zvracením obsahu žaludku. Kojenci se rodí s deformovanou lebkou (vyčnívající čelo, hluboko nasazené oči, příliš dlouhá víčka, silné rty, malý nos). Během prvních měsíců života se čočka posouvá do očí.
Asi 75 procent dosud popsaných případů sulfocysteinurie je způsobeno nedostatkem MoCo: Všechny tři enzymy podílející se na rozkladu síry v těle, siřičitá oxidáza, xantinová oxidáza a aldehyd oxidáza, vykazují velmi sníženou aktivitu. Příčinou nedostatku izolované sulfitové oxidázy je mutace v genu SUOX (chromozom 12). Objevuje se ve třech variantách: typ A (mutace v genu MOCS1), typ B (gen MOCS2) a typ C (gen MOCS3). Nejběžnější je mutace typu A. Inhibuje tvorbu prekurzorové molekuly cPMP. Látka však může být nyní vyráběna a podávána v laboratoři.Za účelem zlepšení doby přežití dětského pacienta by mělo být onemocnění z nedostatku diagnostikováno co nejdříve a mělo by být léčeno každodenním intravenózním podáváním molybdenanu.
Tímto způsobem může být zachyceno alespoň další poškození. Dítěti se podávají antispasmodické léky k potírání záchvatů. Musí být také na dietě s nízkým obsahem bílkovin. Alternativně lze také podávat MoCo prekurzor Z. Snižuje záchvaty a zabraňuje dalšímu poškození mozku. Medicína má velké naděje na léčbu dříve nevyléčitelné nemoci nanočásticemi oxidu molybdenového, které v těle převezmou roli siřičitan oxidázy. Aby se zjistilo, zda nenarozené dítě má nedostatek sulfit oxidázy, může těhotná žena nechat zkontrolovat hladinu S-sulfocysteinu v plodové vodě.

.jpg)






.jpg)



.jpg)